生化分析儀的性能檢定
發(fā)布時間:2017-09-01
自動生化分析儀是由光學、精密機械、電子與計算機技術緊密結合而成的光譜儀器,其結構復雜、技術含量和要求精度高。為了保證生化分析儀分析結果的重復性和準確性,必須對新購買或正在使用的儀器進行性能評價。國家食品藥品監(jiān)督管理局2009年6月1日正式實施的《YY/T0654-2008全自動生化分析儀》醫(yī)藥行業(yè)標準對全自動生化儀的硬件性能提出了具體要求并推薦了檢定的方法。
1.雜散光 首先對儀器進行光電校正(Photocal),隨后在儀器的診斷狀態(tài)下,用50g/L亞硝酸鈉溶液作為測定物質(zhì),用加樣器將溶液直接加入比色杯進行比色,測其在生化儀上相對于蒸餾水在340nm處的吸光度;亦可采用空氣作參比,在340nm處測定JB400型截止型濾光片的吸光度,其值應不小于2.3。
2.溫度準確度測定分析儀預熱自動進入Standby狀態(tài),確保在室溫18~32℃范圍內(nèi),且控制電腦顯示屏上顯示的孵育溫度介于36.8~37.2℃之間,通過加樣孔向比色杯中加入500μl去離子水,5分鐘以后溫度穩(wěn)定。將經(jīng)過標定精度不低于0.1℃溫度的檢測儀探頭固定,確保它和杯底、杯壁都有一定的距離,每隔30秒讀數(shù)一次,連續(xù)觀察20次液晶顯示屏上的溫度顯示值并記錄。求出平均溫度和20次顯示值中最大值與最小值之差,即溫度波動度。溫度應在設定值的±0.3℃內(nèi),波動度不大于±0.2℃。
3.吸光度線性范圍檢定對分析儀340nm和450~520nm范圍內(nèi)任一波長進行線性范圍測定,各個波長的色素原液的配制見表19-1(溶劑中可加表面活性劑0.01%TritonX-100等),色素原液的吸光度應比分析儀規(guī)定的吸光度上限高5%左右。

用相應的稀釋液將色素原液按0/10、l/10、2/10、3/10、4/10、5/10、6/10、7/10、8/10、9/10、10/10的比例稀釋,共獲得11個濃度梯度。各梯度的色素液在分析儀上重復測定5次吸光度,計算平均值。以稀釋比例為橫坐標,吸光度平均值為縱坐標,畫出散點圖,用最小二乘法先對前4個點進行線性擬合,并按照下列公式計算5~11點的相對偏倚。
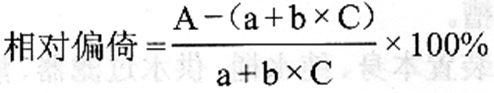
式中:A為某濃度點實際測定的吸光度平均值,a為線性擬合的截距,b為線性擬合的斜率。
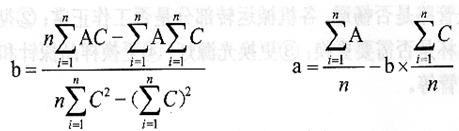
式中:A為某濃度點實際測定的吸光度平均值,C為相對濃度,n為選定的測定點數(shù)。
各測定值的相對偏倚在±5%范圍內(nèi)的最大吸光度應不小于2.0。
4.吸光度穩(wěn)定性檢定對分析儀340nm和600~700nm波長范圍內(nèi)任一波長進行吸光度穩(wěn)定性檢測。340nm吸光度為0.5(蒸餾水為空白,允許偏差為士5%)的重鉻酸鉀標準溶液,600~700nm波長范圍內(nèi)任一波長的測定溶液吸光度為0.5(蒸餾水為空白,允許偏差為±5%)的硫酸銅標準溶液。設定儀器的試劑量為分析儀標稱的最小試劑量、樣本量為標稱的最小樣本量,反應時間為儀器標稱的最長反應時間或10分鐘,讀數(shù)間隔為儀器的測定周期或30秒,測定上述溶液的吸光度,計算其中吸光度最大值與最小值之差,其變化應不大于0.01。
5.吸光度準確度檢定 以蒸餾水作空白對照,以分析儀上測定340nm處吸光度分別約為0.5和1.0(均以蒸餾水為空白對照,允許偏差為±5%)的重鉻酸鉀標準溶液。重復測定3次,計算3次測量值的算術平均值與標準值之差。吸光度為0.5的允許誤差為±0.025,吸光度為1.0的允許誤差應為±0.07。
6.吸光度重復性檢定 對分析儀340nm波長進行吸光度重復性測定。測定溶液340nm吸光度為0.5(蒸餾水為空白對照,允許偏差為土5%)的重鉻酸鉀標準溶液。重鉻酸鉀標準溶液同時作為樣品和試劑,溶液的加入量為分析儀標稱的最小反應體積,反應時間為分析儀標稱的最長反應時問或10分鐘,連續(xù)測定20次,觀察并記錄這20條反應曲線的最后一個讀點的吸光度,計算該點吸光度的變異系數(shù)CV,應不大于1.5%。
7.試劑加樣精確度與重復性檢定 采用稱量法檢測。將生化儀、蒸餾水等置于恒溫、恒濕的實驗室內(nèi)平衡數(shù)小時,準備一帶蓋且先盛有適量蒸餾水的容器并蓋上蓋子防止水分蒸發(fā),在分度值為0.01mg的電子天平上調(diào)零。控制試劑針或樣本針往該容器中加入規(guī)定量的除氣蒸餾水,蓋上蓋子再稱重。每種規(guī)定加入量重復稱量20次,求出均值并除以當時溫度下蒸餾水的密度得到實際加入量(μl),計算加樣誤差:
加樣誤差=(實際加入量一規(guī)定加入量)/規(guī)定加入量×1000%。
儀器標稱的試劑最小、最大加樣量,加樣準確度誤差應不超過士5%,變異系數(shù)應不超過2%。
8.樣品加樣準確性與重復性檢定 可以采用比色法和稱量法兩種檢測方式。稱量法與試劑加樣精確度與重復性檢定類似。比色法是用分度值0.1mg以下的電子天平稱取橘紅G(orange G)粉末0.35g加入10ml質(zhì)控血清中慢慢溶解混勻制成色素原液并測定其比重。
將色素原液加入樣品杯,按儀器加樣量設定范圍分別設定最大加樣量M1、最小加樣量M2,將色素原液重復5次加注不同比色杯中,手工將比色杯內(nèi)色素原液用純水回收到10ml容量瓶中定容,在分光光度計上(478±1):nlrl測定定容后的吸光度A1;同時,將約lml色素原液準確稀釋Dr倍后同樣用分光光度計測定其吸光度Ar。計算實際樣品加注量:
實際加注樣品體積=(M1×A1)/(Dr×Ar)。
計算加樣變異系數(shù)和加樣誤差,結果應符合表19―2的要求。

9.樣品攜帶污染率檢定 用正常人血清溶解適量橘紅G,配制340rim吸光度約為200的原液。將該原液準確稀釋200倍,在分析儀上測定稀釋液在340nm相對于去離子水的吸光度。重復測定20次,計算出平均值,乘以稀釋倍數(shù)獲得橘紅G原液的理論吸光度。以去離子水為試劑,以橘紅G原液和去離子水為樣品,樣品的加入量為分析儀標稱的最大樣品量,按照原液、原液、原液、去離子水、去離子水、去離子水的順序為一組,在分析儀上測定上述樣品反應結束時的吸光度,共進行5組測定。每一組測定中,第4個樣品的吸光度為A14,第6個樣品的吸光度為Ai6為該測定組的序號,按照如下公式計算攜帶污染率:
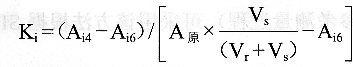
并求出5組的平均攜帶污染率,其值應小于0.5%。
10.臨床項目批內(nèi)與批問精密度檢定采用兩個水平的質(zhì)控血清,針對不同的檢測項目,參照試劑盒質(zhì)量評價時測定批內(nèi)與批問精密度的方式,對不同項目采用某種試劑時的批內(nèi)與批問平均值、SD值及CV值。如ALT<40U/L時CV≤5%、UREA<10mmol/L,時CV≤2.5%、TP 50.0~70.0g/L,時CV≤2.5%方可滿足要求。
11.其他性能檢定 如ISE單元的電極選擇性等也可用廠家提供的電極選擇性測試專用試劑進行檢定。
參考資料:分析化學







