石灰需要量測定
發布時間:2017-09-01
一、分析意義
酸性土壤在我國占有較大的面積,長江以南大部分土壤均屬酸性土壤。土壤酸度基本上是由土壤吸收復合體中交換氫和鋁引起的,酸性過強,往往使鋁、鐵或錳的濃度增高,造成對某些作物的毒害,抑制有益徽生物的活動(如硝化細菌和固氮菌等)。降低了磷素的有效性,還可使某些作物感到鈣素的缺乏。土坡酸堿性的一個重要特點是變異性較大,極易受耕作施肥等人為措施的影響,因此有必要定期測定土坡的酸喊度,并加以改良。對植物生長不利的強酸性土壤,可以通過簡單的措施在極短的時間內改變成中性土壤。常用的方法是施用石灰,以中和土壤的酸性,減少鋁、鐵或錳元素的溶解度,改變土壤吸收復合體中交換性陽離子組成,促進植物根系生長和微生物的活動,活化土壤中的磷索,供給需鈣較多的作物豐富鈣素等。但石灰施得太多就會使一些元素(如鐵、錳)的有效度降低,以致使這些為植物必需的元素呈缺乏狀態。由此可知,準確側定土壤的石灰需要量,把土壤中和至某個特定的pH值或鹽基飽和水準或有毒物質不活化的程度,乃是一個改良酸性土壤極有價值的土壤管理措施,也是提高土鑲肥力,達到作物高產的重要手段之一。
二、方法選擇的依據
酸性土壤石灰需要量是指把土壤從其初始酸度中和到一個選定的中性或微酸性狀態所需的石灰或其它堿性物質的量。測定土壤石灰需要量的方法很多,包括田間試驗法,土壤-石灰培養法,土壤一堿滴定法,土壤一緩沖劑平衡法及作為石灰需要量指標的交換性鋁等。田間試驗法是利用田間對比試驗來決定石灰需要量,此法需要的時間太長,故不常采用。土壤-石灰培養法,在培養過程中,由于微生物活動,常常可導致土壤pH下降.因此要達到平衡,常常超過幾個星期,故是一種費時的方法。土壤一堿滴定法,土壤中的酸性陽離子用堿的標準溶液滴定,但是由于大部分不能立即與堿起反應,因此,直接滴定的過程甚為緩慢,而且不夠準確,但如果先把土壤與較濃的鹽溶液一起混和,滴定過程即可大大加快。土坡一緩沖劑平衡法的產生,是因為直接滴定土壤酸度困難之處,在于如何掌握緩慢加喊使酸能被充分中和,但不致使土坡pH提得過高,而又能使滴定在合理的時間內完成,因此各種緩沖平衡法便應運而生。緩沖平衡法能使土壤酸度在比較低而且近于平衡的pH下面逐漸進行中和。在這些方法中Shoemaker,Mclean與Pratt(簡稱SMP法),Adams與Evans,以及Woodruff等人的方法廣泛應用于美國的各個土壤測定實驗室中,并以此作為測定酸性土壤石灰需要量的基礎。SMP法已被證明特別適用于石灰需要量大于4482 kg/hm2,pH<5.8,有機質<10%,含有大是交換性鋁的土壤。根據SMP緩沖法改進的雙緩沖劑SMP法,研究資料表明,對于陽離子交換量(CEC)很低的土坡和其它低石灰需要量的土壤都有適當的精確度。Adams與Evans方法是側定低CEC土壤和2:1型粘土礦物的土壤石灰需要量的方法,其精度較高,且速度快。在高度風化而且pH低的土壤中,植物生長常常受土壤中鋁的毒害,因此人們建議以中性非緩沖鹽溶液[c(KC1) =1mol?L-1]提取可交換性鋁作為老成土和氧化土石灰需要量的指標。
在眾多石灰需要量的測定方法中,氯化鈣交換-氫氧化鈣中和滴定法,是我國目前側定石灰需要最一個簡便、行之有效的方法,此法模擬了酸性土壤施石灰時引起反應的大致情況,滴定快速,終點明顯,在我國各土壤分析實驗室廣泛采用。對石灰需要量高,而又含有大量可交換性鋁的酸性土壤,可試用SMP單一緩沖劑法。
三、氯化鈣交換-中和滴定法
1、方法原理
用氯化鈣溶液[c (CaCI2)=0.2mol?L-1〕交換出土壤膠體上吸附的氫離子和鋁離子,然后用氫氧化鈣標準溶液滴定其酸度,用酸度計指示終點。根據氫氧化鈣的用童計算石灰需要量。
2、儀器及設備
電位滴定計或酸度計;pH玻璃電極和飽和甘汞電極。
3、試劑
(1)氯化鈣溶液[c(CaC12)=0.2 mol?L-1]:稱取44g抓化鈣(CaC12?6H2O,化學純)溶于水中,稀釋至1L,然后用氮氧化鈣溶液(試劑2)或稀鹽酸調節到pH7.0(用pH計測量)。
(2)氫氧化鈣標準溶液[c?二分之一(Ca(OH)2)]=0.03 mol?L-1〕:稱取4g經9200C灼燒30min的氧化鈣(CaO,分析純)溶于200mL無二氧化碳的水中,攪拌后放置澄清,傾出上部清液于試劑瓶中,用裝有蘇打石灰管及虹吸管的橡皮塞塞緊,用鄰苯二甲酸氫鉀或鹽酸標準溶液標定其濃度。
4、操作步驟
稱取通過2mm篩孔的風干土樣10. 00g于100mL燒杯中,加入氯化鈣溶液(試劑1)在磁力攪拌器上充分攪拌1min,插人pH玻璃電極和飽和甘汞電極,邊攪拌邊用氫氧化鈣標準溶液(試劑2)滴定,直到酸度計(或電位計)上的指針指在pH7.0時為終點,記錄消耗的氫氧化鈣標準溶液mL數。
5、結果計算
石灰需要量以中和每公頃耕層土壤(200~260萬kg)需要用氧化鈣(即生石灰,CaO)的kg數計算。但實驗室測定條件與田間實際情況的差異,施石灰的計算方法為:
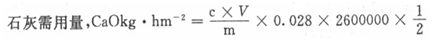
式中:c――滴定用氫氧化鈣標準溶液的濃度,mol?L-1;
V――滴定樣品時用去氫氧化鈣標準溶液的體積,mL;
m―土樣的質量,g;
0.028――氧化鈣(二分之一CaO)的摩爾質量,kg/mol;
2600000――每公頃(hm2)耕層(20cm)土壤的質量,kg;
二分之一――實驗室測定條件與田間實際施用情況差異的校正系數。
4、SMP緩沖劑法(試用)
(1)方法原理
一種緩沖溶液通常就是一種弱酸和同種弱酸的鹽的混合物。這種緩沖溶液既能中和酸也能中和堿,因此能防止系統中的pH的劇烈變化。加人一種酸性物質而引起的緩沖液pH的線性變化,則可用于指示出以緩沖液pH變化而代表的總酸度。由于酸性土坡本身就是一個緩沖劑,所以當土壤加入混合緩沖液中時,由此產生的雙緩沖懸浮液(土鑲一緩沖劑)必然是較為復雜的。最初提出的SMP緩沖劑法,是以一些土類中的緩沖一指示石灰搖要盆和CaCO3培養測定石灰需要量之間的相關關系作為根據。但土壤和緩沖液混合過程中產生緩沖液pH變化是很復雜的,主要是因為大部分酸度是pH依變酸度,而且只有總酸度的一部分與緩沖液發生反應。因此在土壤-緩沖液的pH值高于6.9,有機質含量高或在酸性淋溶土壤中,用SMP方法測出的石灰需要量易產生誤差。
(2)儀器及設備
pH計;玻璃電極;飽和甘汞電極。
(3)試劑SMP緩沖液配制
①稱取32.4g對硝墓酚, 54.0g鉻酸鉀(K2CrO4), 955.8g抓化鈣(CaCI2?2H20)于18L容器中。
②加人約9L蒸餾水,邊加水邊強烈振蕩,并繼續振蕩數分鐘以防鹽分表面結殼。
③稱取36.0g乙酸鈣〔Ca(OAc)2]于另一容器中,加5L左右燕餾水溶解。
④將溶液3加到溶液2中,然后振蕩混勻,每隔15min-20min振蕩一次,共需振蕩2h~3h。
⑤加人45mL三乙醇胺(TEA),加人時不斷振蕩。
⑥間歇振蕩使混合物完全溶解,約需8h。
⑦用燕餾水稀釋至18L。
⑧用校正好的pH計以氮氧化鈉溶液[p(NaOH)=150g?L-1]調節至pH 7.5。
⑨用玻璃纖維片(或棉墊)進行過濾。
⑩用干操劑和蘇打石灰隔絕二氧化碳和水汽,以防止CO2和水汽的污染。
(4)操作步驟
校正pH計。由于SMP緩沖劑已調節至pH7.5,并有防污染措施,故pH每日變化很小,可作為一種二級標準液用于pH正常操作的校正。
稱取通過2mm篩孔風干土樣5.00g于50 mL離心管,加5mL燕餾水,混合并攪拌1min,靜置30min,側定該溶液pH值。然后加人SMP緩沖液10mL。
把離心管蓋上蓋子放在振蕩機上,以250振次/min振蕩10min,靜置30 min。或者振蕩15min,靜置15min,然后側定pH值。振蕩時間,放置時間,以及振蕩強度(如振次250次/min到低至200次/min時)對土壤緩沖液的pH讀數會有些影響。用搖動電極來攪拌土壤懸液,在校正好的pH計上讀出pH值,并記錄土壤-緩沖液pH。
5、結果計算
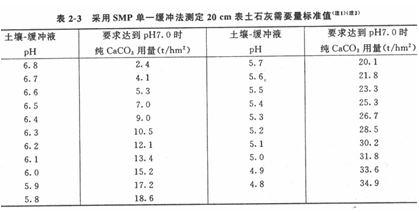
根據側得的土壤-緩沖液pH,由表2-3查出石灰需要量并記錄。
6、注意事項
(1)如果耕層深度不是20cm,則應根據20cm的深度變化比例,增加或減少石灰需要量的數值。
(2)表中所列系純CaCO3量,如非純碳酸鈣,則需調整。
參考資料:土壤農業化學分析方法







