首頁(yè)>技術(shù)中心>技術(shù)資訊>選煤用磁鐵礦粉試驗(yàn)方法(二)
選煤用磁鐵礦粉試驗(yàn)方法(二)
發(fā)布時(shí)間:2017-09-01
五、磁性物含量的測(cè)定
1.方法提要
采用磁選管法測(cè)定試樣的磁性物含量。磁選管法的工作原理是在C形電磁鐵的兩極之間裝有玻璃管,并作往復(fù)移動(dòng)和旋擺運(yùn)動(dòng)。當(dāng)磁選管中的試樣通過(guò)磁場(chǎng)區(qū)時(shí),磁性物即附著于管壁,非磁性物在機(jī)械運(yùn)動(dòng)中被水沖刷而排出,使磁性物與非磁性物分離。以磁性物質(zhì)量占試樣質(zhì)量的百分比來(lái)表示磁性物含量。
2.測(cè)定步驟
①根據(jù)取樣要求縮取(20.00±0.02)g試樣,將試樣裝入一個(gè)容積為1000mL的燒杯中,加入適量酒精和約500mL水,攪勻并靜置約5min,攪拌時(shí)要確保顆粒被充分地潤(rùn)濕。
②組裝全套裝置,接通電源,調(diào)節(jié)激磁電流使其達(dá)到預(yù)定的磁場(chǎng)強(qiáng)度。向磁選管中加水直至距漏斗處約5cm,然后將燒杯中的混合物緩慢地倒入漏斗,打開(kāi)磁選管下面的螺旋夾,使液體以50mL/min的流量流人容積為2500mL的燒杯中。磁選管在運(yùn)動(dòng)中,非磁性物隨水流下沉直至排出管外,磁性顆粒將附著于兩磁極處管壁內(nèi)。為使被吸持的磁鐵礦粉始終浸沒(méi)在水中,必要時(shí)向漏斗中加水。
③將螺旋夾關(guān)閉,關(guān)閉激磁電源,使被吸持的磁性物脫開(kāi),打開(kāi)螺旋夾,將磁性物沖入一個(gè)500mL的燒杯中。當(dāng)磁性物完全沉淀后,慢慢倒出燒杯中的水,同時(shí)用一塊強(qiáng)磁鐵放在燒杯杯底,以防止杯中磁性物有任何損失。
④打開(kāi)激磁電源,關(guān)閉螺旋夾,向磁選管中加水。打開(kāi)螺旋夾,使水流動(dòng),把第一個(gè)2500mL燒杯中的液體和固體慢慢地加入漏斗,使混合液通過(guò)磁選管進(jìn)入第二個(gè)2500mL燒杯,并收集由磁鐵吸持的磁鐵礦粉。
⑤檢查第二個(gè)2500mL燒杯中的液體中有無(wú)殘存的磁性物,方法是將其放在一塊強(qiáng)磁鐵上,使燒杯慢慢移動(dòng),觀察其中有無(wú)磁性顆粒,如果杯中沒(méi)有磁性物,將杯中液體倒掉。如果發(fā)現(xiàn)還有磁性物,應(yīng)將杯中液體倒回磁選管,使其再通過(guò)一次檢查,直至杯中不存在磁性物為止。
⑥將一個(gè)空的2500mL燒杯放在磁選管下,向磁選管中加水沖洗被磁鐵吸持的磁性物(在關(guān)閉激磁電源后),將磁選管拆下并左右轉(zhuǎn)動(dòng),直至排出的液體變清。按步驟③所述方法回收磁鐵礦粉,并將其收集至一個(gè)500mL的燒杯中。
⑦每次用步驟⑥收集的2500mL燒杯中的固液混合物,重復(fù)步驟④、⑤、⑥,直至步驟④中沒(méi)有磁性物被磁極吸持住為止。
注:為充分完成該過(guò)程,一般需做兩個(gè)循環(huán)。
⑧把收集的全部磁性物干燥到質(zhì)量恒定狀態(tài),在干燥器中取出后立即稱量,精確到±10mg。
3.結(jié)果計(jì)算
用磁性物和試樣的質(zhì)量百分比來(lái)表示磁性物含量,其計(jì)算公式如下式:
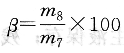
式中β――磁性物含量,%;
m7――試樣質(zhì)量,g;
m8――磁性物質(zhì)量,g。
平行測(cè)定允許差為0.5%(絕對(duì)差值)。報(bào)告結(jié)果精確到小數(shù)點(diǎn)后一位。
六、相對(duì)密度的測(cè)定
1.方法提要
使磁鐵礦粉試樣在密度瓶中潤(rùn)濕沉降并排除吸附的氣體,根據(jù)試樣排出的同體積的水的質(zhì)量算出磁鐵礦粉的真相對(duì)密度。
2.試樣
應(yīng)采用在105~110℃溫度下干燥至質(zhì)量恒定的試樣進(jìn)行測(cè)定。按取樣要求,二次取樣。從干燥的試樣中縮取不少于15g,用作待測(cè)試樣。
注:試樣中有任何水分,都會(huì)使測(cè)得的密度有較大誤差。
3.測(cè)定步驟
①稱帶瓶塞的密度瓶的質(zhì)量,然后將試樣放入瓶中,蓋上瓶塞再稱量,兩次稱量均準(zhǔn)確至1mg。
②往密度瓶?jī)?nèi)加入半瓶水,將瓶放到抽氣容器中抽出夾在磁鐵礦粉中的空氣,然后讓空氣逐漸地進(jìn)入容器。
③從抽氣容器中取出密度瓶,并加入脫氣的水,直至接近加滿。
注:不能將瓶子完全加滿,以便液體在溫度平衡中有膨脹余地。
④把密度瓶放入水浴中,將溫度控制在(25.0±0.1)℃至少45min。當(dāng)瓶子還在水浴中時(shí)蓋上瓶塞(不要夾帶任何氣泡)。然后用濾紙除掉瓶塞頂上的過(guò)量水。
⑤把瓶子從水浴中取出并擦干瓶子表面帶的水分。要特別注意不要使瓶中的液體由于外部壓力或因?yàn)槭职哑孔蛹訜岫绯觥?/p>
⑥稱量帶瓶塞和水及試樣的密度瓶的質(zhì)量,準(zhǔn)確至1mg。
4.標(biāo)定(空白試驗(yàn))
標(biāo)定用蒸餾水進(jìn)行。標(biāo)定步驟基本和上述測(cè)定步驟相同,不同的是瓶?jī)?nèi)僅加蒸餾水。標(biāo)定要特別仔細(xì),將瓶子從水浴中取出至最后稱量的時(shí)間間隔越短越好。這樣可以使因瓶子受熱產(chǎn)生對(duì)流作用和瓶中液體蒸發(fā)造成的誤差降至最低。
5.結(jié)果計(jì)算
25℃溫度下磁鐵礦粉的真相對(duì)密度可通過(guò)下式算出:
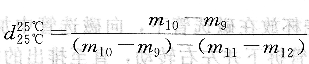
式中 d25℃25℃――25℃時(shí)磁鐵礦粉的真相對(duì)密度;
m9――密度瓶和瓶塞的質(zhì)量,g;
m10――密度瓶和瓶塞加試樣的質(zhì)量,g;
m11――密度瓶和瓶塞加試樣和蒸餾水的質(zhì)量,g;
m12――密度瓶和瓶塞加蒸餾水的質(zhì)量,g。
應(yīng)計(jì)算出兩次平行測(cè)定結(jié)果的平均值。報(bào)告結(jié)果精確到小數(shù)點(diǎn)后兩位。
七、全鐵含量的測(cè)定
1.方法提要
試樣用鹽酸分解,過(guò)濾,濾液作為主液保存;殘?jiān)詺浞岢瑁沽蛩徕浫廴冢}酸浸取,用氫氧化銨使鐵沉淀,過(guò)濾,沉淀用鹽酸溶解并與主液合并。用氯化亞錫還原,再用氯化汞氧化過(guò)剩的氯化亞錫,以二苯胺磺酸鈉為指示劑,用重鉻酸鉀標(biāo)準(zhǔn)溶液滴定,以此測(cè)定全鐵量。
2.試樣
①一般試樣粒度應(yīng)小于100μm,如試樣中結(jié)合水或易氧化物質(zhì)含量高時(shí),其粒度應(yīng)小于160μm。
②預(yù)干燥不影響試樣組成者應(yīng)按GB 6730.1―86《鐵礦石化學(xué)分析方法 分析用預(yù)干燥試樣的制備》進(jìn)行。
3.測(cè)定
(1)測(cè)定數(shù)量 同一試樣,在同一實(shí)驗(yàn)室,應(yīng)由同一操作者在不同時(shí)間內(nèi)進(jìn)行2~4次測(cè)定。
(2)試樣量 稱取0.2000g試樣。
(3)空白試驗(yàn) 隨同試樣做空白試驗(yàn),所用試劑須取自同一試劑瓶。
(4)校正試驗(yàn) 隨同試樣分析同類(lèi)(指測(cè)定步驟相一致)的標(biāo)準(zhǔn)試樣。
(5)測(cè)定步驟
①試樣的分解。將試樣置于400mL燒杯中,加入30mL鹽酸(ρ=1.19g/mL),低溫加熱(應(yīng)控制在1050C以下)分解,待溶液體積至10~15mL時(shí)取下,加溫水至溶液量約40mL,用中速濾紙過(guò)濾,用擦棒擦凈燒杯壁,再用熱水洗燒杯3~4次、殘?jiān)?~6次,將濾液和洗液收集于500mL燒杯中,作為主液保存。
將濾紙連同殘?jiān)?sup>①置于鉑坩堝中,灰化,在800℃左右灼燒20min,冷卻,加水潤(rùn)濕殘?jiān)?滴硫酸(1+1)、5mL氫氟酸(ρ=1.15g/mL),低溫加熱,蒸發(fā)至三氧化硫白煙冒盡,取下。加3g焦硫酸鉀,在650 0C左右熔融約5min,冷卻,置于400mL燒杯中,加50mL鹽酸(1+10)緩慢加熱浸取,熔融物溶解后,用溫水洗出鉑坩堝②。加熱至沸,加2滴甲基橙溶液(0.1%),用氫氧化銨(ρ=0.90g/mL)慢慢中和至指示劑變黃色,過(guò)量5mL,加熱至沸,取下。待沉淀下降后,用快速濾紙過(guò)濾,用熱水洗至無(wú)鉑離子[收集洗滌8次后的洗液約10mL,加lmL鹽酸(1+1)、1 0滴氯化亞錫溶液,溶液無(wú)色,即表明無(wú)鉑離子],用熱鹽酸(1+2)將沉淀溶解于原燒杯中,并洗至無(wú)黃色,再用熱水洗3~4次,將此溶液與主液合并③。低溫加熱濃縮至約30mL。
②還原、滴定。趁熱用少量水沖洗杯壁,立即在攪拌下滴加氯化亞錫溶液(6%)至黃色消失,并過(guò)量1~2滴,冷卻至室溫,加人5mL氯化汞飽和溶液,混勻,靜置3min,加150~200mL水,加30mL硫磷混酸、5滴二苯胺磺酸鈉溶液(0.2%),立即以重鉻酸鉀標(biāo)準(zhǔn)溶液(0.008333mol/L)滴定至穩(wěn)定紫色。
③空白測(cè)定。空白試液滴定時(shí),在加硫磷混酸之前,加入6.00mL硫酸亞鐵銨溶液,滴定后記下消耗重鉻酸鉀標(biāo)準(zhǔn)溶液的體積(A),再向溶液中加入6.OOmL硫酸亞鐵銨溶液,再以重鉻酸鉀標(biāo)準(zhǔn)溶液滴定至穩(wěn)定紫色,記下滴定的體積(B),則V0=A-B即為空白值。
4.結(jié)果計(jì)算
(1)全鐵含量的計(jì)算 按下式計(jì)算全鐵的含量TFe(%):
式中 V――試樣消耗重鉻酸鉀標(biāo)準(zhǔn)溶液的體積,mL;
V0――空白試驗(yàn)消耗重鉻酸鉀標(biāo)準(zhǔn)溶液的體積,mL;
m――試樣量,g;
0.0027925――與1mL O.008333mol/L重鉻酸鉀標(biāo)準(zhǔn)溶液相當(dāng)?shù)蔫F量,g;
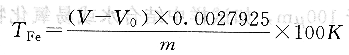
由公式![]() 所得的換算系數(shù)(如使用預(yù)干燥試樣則K一1),A是按照國(guó)家標(biāo)準(zhǔn)測(cè)定得到的吸濕水質(zhì)量分?jǐn)?shù)。
所得的換算系數(shù)(如使用預(yù)干燥試樣則K一1),A是按照國(guó)家標(biāo)準(zhǔn)測(cè)定得到的吸濕水質(zhì)量分?jǐn)?shù)。
(2)分析值的驗(yàn)收 當(dāng)平行分析同類(lèi)型標(biāo)準(zhǔn)試樣所得的分析值與標(biāo)準(zhǔn)值之差不大于表3-30所列的允許差時(shí),則試樣分析值有效,否則無(wú)效,應(yīng)重新分析。分析值是否有效,首先取決于平行分析的標(biāo)準(zhǔn)試樣的分析值是否與標(biāo)準(zhǔn)值一致。
當(dāng)所得試樣的兩個(gè)有效分析值之差不大于表3-30所列允許差時(shí),則可予以平均,計(jì)算為最終分析結(jié)果;如二者之差大于允許差,則應(yīng)按驗(yàn)收試樣分析值程序(見(jiàn)圖3-4,圖中,即表3-30中所列試驗(yàn)允許差),進(jìn)行追加分析和數(shù)據(jù)處理。

(3)最終結(jié)果的計(jì)算 試樣的有效分析值的算術(shù)平均值為最終分析結(jié)果。平均值計(jì)算至小數(shù)點(diǎn)后第四位,并按數(shù)字修約規(guī)則的規(guī)定修約至小數(shù)點(diǎn)后第一位。
八、鐵(Ⅱ)含量的測(cè)定
1.方法原理
在氮?dú)夥罩杏名}酸溶解試樣,然后用標(biāo)準(zhǔn)的重鉻酸鉀溶液滴定鐵(Ⅱ)。
2.測(cè)定步驟
①稱取O.25g經(jīng)過(guò)空氣干燥的試樣(精確到1mg)并將其放人反應(yīng)瓶中。為了把鐵 (Ⅱ)的測(cè)定結(jié)果校正為干基,進(jìn)行空氣干燥水分的測(cè)定。
②把冷卻器裝到燒瓶上,把滴液漏斗裝到側(cè)瓶頸上,把氣體導(dǎo)入管接在滴液漏斗上,并與供氮?dú)獾臍庠唇由希昧髁繛?00mL/min的氮?dú)膺M(jìn)行吹洗至少5min。
③關(guān)閉滴液漏斗的旋塞閥,拿掉氣體導(dǎo)入管。向滴液漏斗中加入25mL鹽酸溶液。重新接上氮?dú)鈿庠矗蜷_(kāi)旋塞閥,使氮?dú)鈱Ⅺ}酸送人燒瓶,繼續(xù)以500mL/min的流量通入氮?dú)狻?/p>
④在氮?dú)饬髦休p微沸騰10min,把燒瓶從電爐上取下,摘去冷卻器。在繼續(xù)通氮?dú)庀聦恐糜谒壑欣鋮s。
⑤冷卻后,加入100mL正磷酸溶液和5滴二苯胺磺酸鹽指示劑,繼續(xù)通氮?dú)狻?/p>
⑥在通氮下用標(biāo)準(zhǔn)重鉻酸鉀溶液不斷滴定,直到加入1滴重鉻酸鉀溶液,顏色由綠變成紫紅且搖勻后顏色不變?yōu)橹埂?/p>
3.結(jié)果計(jì)算
以氧化亞鐵(FeO)質(zhì)量與試樣質(zhì)量的百分比來(lái)表示鐵(Ⅱ)含量,計(jì)算公式如下式:

式中 FeO(干基)――鐵(Ⅱ)含量,%;
c――重鉻酸鉀溶液的物質(zhì)的量濃度,
V――在滴定中消耗重鉻酸鉀的體積,
71.85――氧化亞鐵的摩爾質(zhì)量,g/mol。
注:試樣中以硫化鐵形式存在的硫化物硫會(huì)影響測(cè)定效果。為了校正,必須測(cè)定硫化物硫。0.2%的硫化物硫會(huì)造成0.25% FeO的正偏差。報(bào)告結(jié)果精確到0.5%(絕對(duì)值)。
參考資料:煤質(zhì)分析及煤化工產(chǎn)品檢測(cè)







